RS Safra 2025/26: chuvas atrasam colheita da soja
Umidade elevada reduz qualidade dos grãos e amplia perdas em áreas do estado
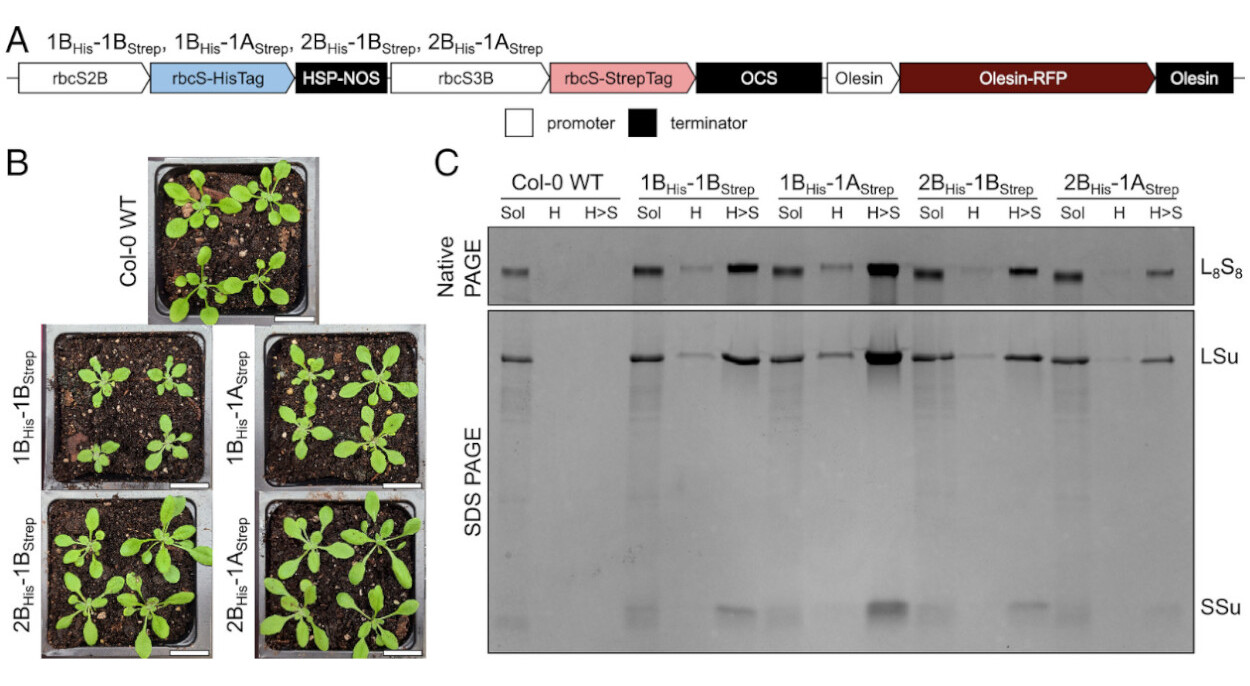
A composição das subunidades da enzima Rubisco altera sua eficiência fotossintética em resposta à temperatura. Estudo demonstrou que plantas modulam pequenas subunidades para ajustar atividade catalítica e estabilidade estrutural. O trabalho utilizou Arabidopsis thaliana como modelo e identificou heterogeneidade no holoenzima como fator central na aclimatação térmica.
A Rubisco, abreviação de Ribulose-1,5-bisfosfato carboxilase/oxigenase, catalisa a fixação de CO2 no ciclo de Calvin. A enzima apresenta estrutura L8S8, com oito subunidades grandes e oito pequenas. Pesquisadores demonstraram que diferentes pequenas subunidades podem coexistir no mesmo complexo. Essa combinação gera múltiplas configurações estruturais. Mais de 50% da Rubisco analisada apresentou heterogeneidade quando expressa em sistema heterólogo.
A equipe identificou pelo menos quatro proporções distintas entre subunidades pequenas no holoenzima. Essa variação altera propriedades cinéticas. Resultados indicaram efeito linear sobre a velocidade máxima de carboxilação (Vcmax). Em contraste, afinidade por substrato (Km para RuBP) apresentou resposta antagonista. A Rubisco heterogênea exibiu menor afinidade por substrato e maior taxa de liberação de inibidores.
Dados estruturais obtidos por criomicroscopia eletrônica mostraram diferenças na flexibilidade do sítio ativo. Subunidades associadas a temperaturas elevadas promoveram maior rigidez local. Subunidades associadas a temperaturas baixas aumentaram flexibilidade. Essa modulação estrutural impacta diretamente a eficiência catalítica.
Segundo descrição do estudo, plantas ajustam a “configuração externa” da Rubisco conforme temperatura. Em ambiente frio, a enzima assume conformação mais flexível e rápida. Em ambiente quente, adota conformação mais rígida, com maior estabilidade e menor risco de reações indesejadas.
A expressão gênica das subunidades pequenas varia com temperatura. Em plantas cultivadas a 10 ºC, subunidades do tipo A predominam. Em plantas a 30 ºC, subunidades do tipo B dominam. Essa mudança altera parâmetros como afinidade por CO2 e taxa catalítica.
O mecanismo identificado envolve ajuste fino da estabilidade local do sítio ativo. Subunidades do tipo B aumentam estabilidade em altas temperaturas. Esse efeito reduz fotorrespiração e melhora eficiência de fixação de carbono. Subunidades do tipo A favorecem maior flexibilidade em baixas temperaturas, elevando velocidade de reação.
A presença de Rubisco heterogênea sugere papel adicional na adaptação. A combinação de subunidades distintas permite respostas intermediárias. Esse arranjo amplia a faixa térmica de funcionamento da enzima. Contudo, menor afinidade por substrato indica possível custo fisiológico.
Outras informações em doi.org/10.1073/pnas.2519914123

Receba por e-mail as últimas notícias sobre agricultura